本文是一篇临床医学论文,笔者经过研究,得出以下结论:DTC术后131I治疗后患者24h全身残留放射性活度、甲状腺动静态显像阳性率与半年后清甲成功有关,可为患者后续的个体化治疗提供参考依据。
1材料与方法
1.1研究对象
本研究为前瞻性研究。研究对象为2020年1月至2021年7月期间,在桂林医学院附属医院DTC术后首次接受131I治疗患者,共接受108例患者,符合纳排标准纳入研究共计84例。其中女性57例(67.90%),男性27例(32.10%),男女比例1:2.11,年龄15-67(41.20±11.72)岁。所有患者在行131I治疗前收集患者个体特征指数,如性别、年龄、体重指数(bodymass index,BMI)、肝功能、血脂、甲状腺动静态显像。131I治疗后均行0、2、4、6、24、48、72h的全身残留放射性活度显像。本研究经我院伦理委员会批准(YJSLL2021118),且所有患者均自愿参与并签署知情同意书。
纳入标准:已行甲状腺近全切或次全切切除术,病理结果证实为DTC;入院为首次行131I治疗者,且TSH>30μIU/ml;具有完整相关临床资料。排除标准:行甲状腺部分切除或单叶切除术;病例为其他类型甲状腺癌;入院为复次131I治疗者;相关临床资料不全者。
........................
1.2药物及仪器
1.2.1放射性131I治疗
所有患者131I治疗前禁碘饮食1个月,停服左旋甲状腺素或甲状腺素片3-4周。依据美国ATA指南[18]治疗剂量3.7-5.5GBq,由两名及以上主治医师共同决定治疗剂量。131I是由北京原子高科公司提供。
.............................
2结果
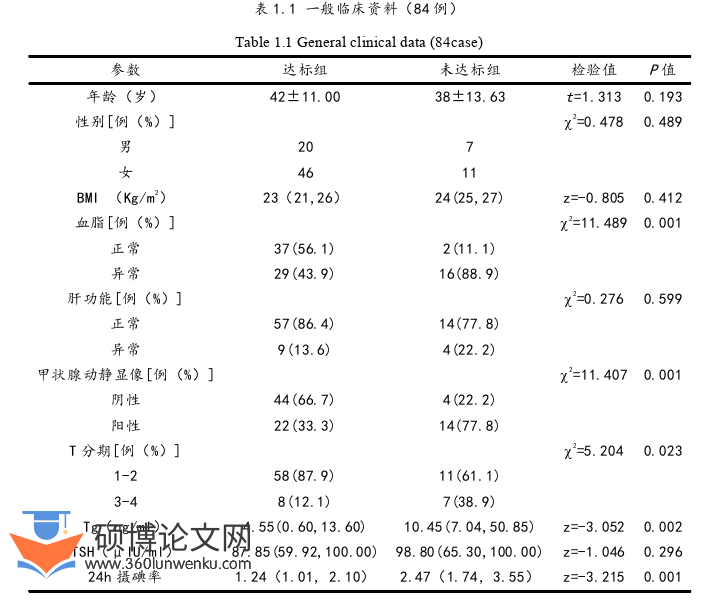
2.1一般临床资料比较(见表1.1)
84例DTC术后131I治疗后患者中,48h体内残留放射性活度达出院标准66例,未达标组18例,48h患者出院率为78%(66/84)。在所有患者T分期中,1期50例,2期19例,3期12例,4期3例;低危组74例,中危组10例。达标组48h体内残留放射性活度211.64(155.03,278.88)MBq低于未达标组489.14(437.52,619.65)MBq差异有统计学意义(z值:-6.476,P<0.05)。
临床医学论文参考
...........................
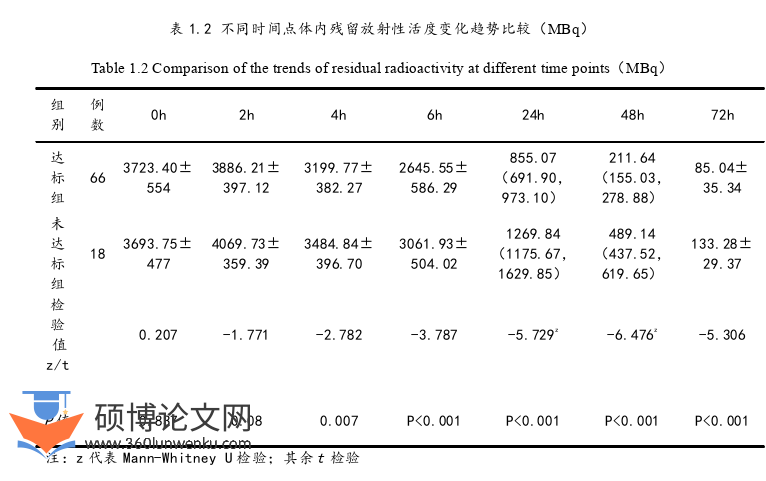
2.2不同时间点体内残留放射性活度变化趋势比较
如表1.2所示,两组患者在0、2h体内残留放射性活度差异无统计学意义(t值:0.207、-1.771,P>0.05),达标组患者131I治疗后患者在4、6、24、48、72h体内残留放射性活度分别为3199.77±382.27、2645.55±586.29、855.07(691.90,973.10)、211.64(155.03,278.88)、85.04±35.34MBq;显著低于未达标组3484.84±396.70、3061.93±504.02、1269.84(1175.67,1629.85)、489.14(437.52,619.65)、85.04±35.34、133.28±29.37MBq;t值:-5.306~-2.782,z值:-5.729、-6.476,P<0.05)。所有患者72h体内残留放射性活度小于400MBq。
临床医学论文怎么写
..........................
2结果……………………………….29
2.1一般临床资料比较……………………….29
2.2两组全身残留放射性活度比较………………....29
2.3两组头颈部残留放射性活度比较……………….…….30
2.4两组二元Logistic回归分析……….......……………30
2.5甲状腺动静态显像阴性组单因素回归分析………………….31
3讨论…………………………..32
4结论…………………………34
3讨论
DTC是最常见的内分泌恶性肿瘤,也是女性中最常见的癌症之一。Benua等[22]在20世纪60年代初首次把131I治疗方法应用于成人甲状腺癌。131I释放β射线,对DNA、RNA、蛋白质和脂质等造成不可恢复的损害,最终导致细胞死亡,而碘作为合成甲状腺最主要的原料,其同族元素131I也可被甲状腺摄取,利用这一原理131I被广泛用来治疗DTC[22、23]。电离辐射主要通过产生活性氧引起细胞DNA损伤,从而造成细胞损伤[24]。然而131I治疗期间,131I对健康细胞DNA的严重辐射损伤,增加了继发性癌症可能性。DTC术后131I治疗后患者体内具有放射性,因此有必要对131I治疗后患者进行隔离治疗,从而减轻对周围人群及医务人员可产生电离辐射危害。不同国家制定的标准不同,我国卫生健康委员会规定DTC术后131I治疗后患者体内残余辐射小于400MBq才符合出院标准[17]。从患者剂量学和辐射防护的角度来看,131I治疗后患者体内残留放射性活度测定作为出院标准的重要参考因素值得我们注意。
国内外学者对DTC术后131I治疗后患者体内残留放射性活度的评估测定开展了一系列研究,大多是通过外部剂量当量率和间接估算法[26-29]。汤敏敏等[26]通过不同时间点尿液总活度间接估算患者体内的残留活度。Eberlein等[29]通过在0.5至120h之间获得至少7个外周血样本,绘制血液和全身的时间-活性曲线,估算出患者体内残留131I活度。国内靳平燕等[30]、袁海娟等[31]通过测量患者的辐射剂量率估计出院时间。Abuqbeitah等[32]研究显示通过患者血液样本可间接评估转移性DTC放射性碘治疗中辐射剂量活性。局部测量法凭借其体积小,测量时间短,而被临床医师广泛应用于评估患者出院时间,但测量1m的距离,使其结果易受外界环境的干扰,且其测量范围有一定限度。尿液测量法不仅增加医务人员辐射损害,而且易受到胃肠道等相关因素影响往往导致测量结果不准确。血液剂量测定法可测量患者血液放射性活度,确保达到治疗功效的前提下不超过安全剂量,提高患者总体生存率,但其具有创伤性,需患者依从性较高,增加医务人员额外辐射。而全身辐射检测系统可大剂量实时显像并直接获得全身残留放射性活度。季艳会等[33]和韩瑜芙等[34]采用全身辐射检测系统直接测量患者体内残余辐射活度,与本文研究测量仪器一致。
..............................
4.结论
(1)131I治疗后患者第一天代谢最快,尤其是前6h,本研究48h患者达标出院率为78%。
(2)对DTC术后首次131I治疗后患者体内残留放射性活度产生影响的独立因素包括:血脂、甲状腺动静态显像、24h摄碘率。在临床上对于血脂异常,甲状腺动静态显像异常以及24h摄碘率较高的患者,应注意48h患者达不到出院标准的可能性越大。这一研究将会对公众辐射防护、医疗资源的合理利用和提高患者的个体化管理将起到重要作用。
参考文献(略)
