本文是一篇临床医学论文,本实验收集的样本量为27例,其中成功并进行分析的有19例,样本量并不是特别充足,导致CD8+T细胞群在TILs和外周血中的比例可能会有偏倚,导致结果出现误差。
第一章 前言
1.1 肝细胞癌的发病机制及治疗现状
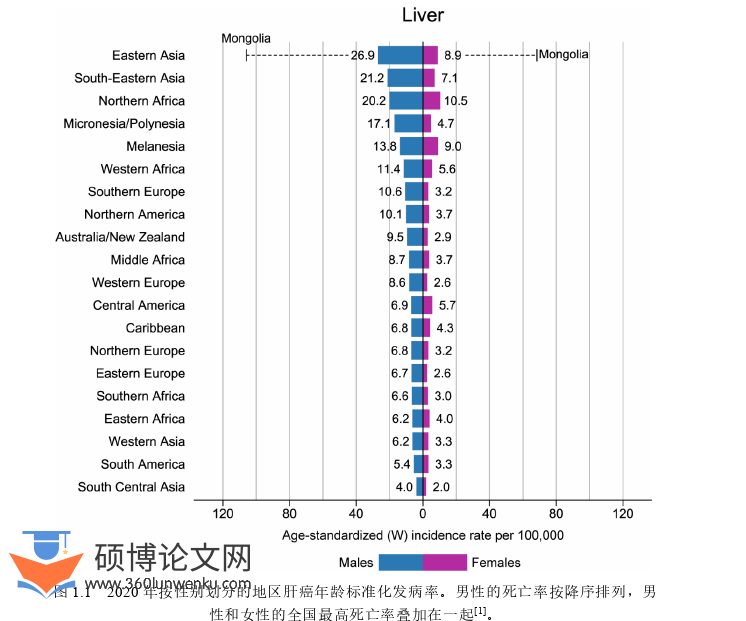
原发性肝癌(Primary liver cancer,PLC)是现有癌症类型中的主要角色之一,其恶性程度,发病率,致死率一直居高不下。从全世界的角度来看,以新发病例为标准,PLC在所有肿瘤类别中排名第六,以肿瘤的死亡率为指标,PLC在所有癌症类型中排名第三。仅2020年全球就有906000新发病例和830000例死亡病例,其中男性患者通常是女性患者的2-3倍(图1.1)。PLC的类型以肝细胞肝癌(Hepatocellular carcinoma,HCC)为主,其占病例的75%-85%左右,第二大常见类型以肝内胆管细胞癌(Intrahepatic cholangiocarcinoma,ICC)为主,其占病例的10-15%,其余是一些罕见类型[1]。
临床医学论文参考
.........................
1.2 基于T淋巴细胞的免疫疗法的发展和应用
随着科学家们逐渐深入的研究,发现免疫治疗或许是解决癌症问题的终极方案。2018年,诺贝尔生理或医学奖颁发给了Tasuku Honjo和James P. Allison,因为他们在“发现负性免疫调节治疗癌症的疗法”方面有了突破性的研究,让免疫疗法能够应用于临床。这证明了免疫疗法相关研究确实有了实质性的突破。目前免疫疗法主要方式包括免疫检查点抑制剂(Immune checkpoint inhibitors,ICI)、过继细胞转移疗法(Adoptive cell therapy,ACT)、细胞因子疗法、溶瘤病毒疗法和癌症疫苗等(图1.3)。
无论是HCC还是其他癌症,本质都是一种基因组疾病,其特征是基因组非常不稳定,在其发生发展的过程中会产生大量的突变[5]。在积累了一定的突变后,癌细胞慢慢产生了肿瘤抗原,这些抗原最终被免疫系统捕获,从而产生了免疫反应。收到信号激活的免疫细胞通过各种方式渗透到肿瘤微环境(Tumor microenvironment,TME)中,参与杀伤肿瘤[6]。人体有效的免疫应答可以正常杀死肿瘤细胞,在其未发展成肿瘤组织就将其扼杀在摇篮里。同时也可以损伤肿瘤细胞的功能和表型,延缓其持续发展[7]。不幸的是,目前肿瘤能够成为导致人类死亡的第一大原因是肿瘤细胞已经进化出了多种机制来抑制或抵抗人自身的免疫反应,例如聚集免疫抑制细胞群来抵御免疫细胞的杀伤,抗原提呈机制的缺陷以逃避免疫系统监视,负调控通路上调以减弱免疫反应等[8-12]。
免疫疗法旨在增强自然防御能力,让免疫系统能够杀死肿瘤细胞,这样比手术切除等物理方法去除癌症更温和,效果更好,副作用小,甚至能够治愈肿瘤。尽管让自身免疫系统来根除癌症的想法在一百年前就已经提出[13, 14],但最近的基础研究和临床研究才有了一些重大进展。尽管其疗效有限,机制目前还没有研究清楚,但目前多种癌症已经对免疫治疗表现出有效的临床效果[15-20]。免疫细胞是免疫系统的武器,因此,TME中的细胞是了解免疫水平和肿瘤免疫状态的关键,尽管TME中的环境特别复杂,但是对于关键细胞群的分析,例如T细胞群,就可以一探肿瘤免疫的秘密所在。
............................
第二章 材料与方法
2.1 HCC组织标本信息
27例肝细胞肝癌患者中男22例,女5例,年龄36~69岁,所有纳入患者均有明确的病理诊断,且均来自兰州大学第一医院。肝切除术前均未经过肿瘤消融、肝动脉化疗栓塞术(Transcatheter arterial chemoembolization,TACE)、放射治疗、化疗以及免疫治疗。样本均取自肝细胞癌患者手术后切下的肿瘤标本,切取距离肝细胞癌包膜2cm以内的肿瘤组织。本研究已通过医院伦理委员会批准(LDYYLL2023-54)。
...........................
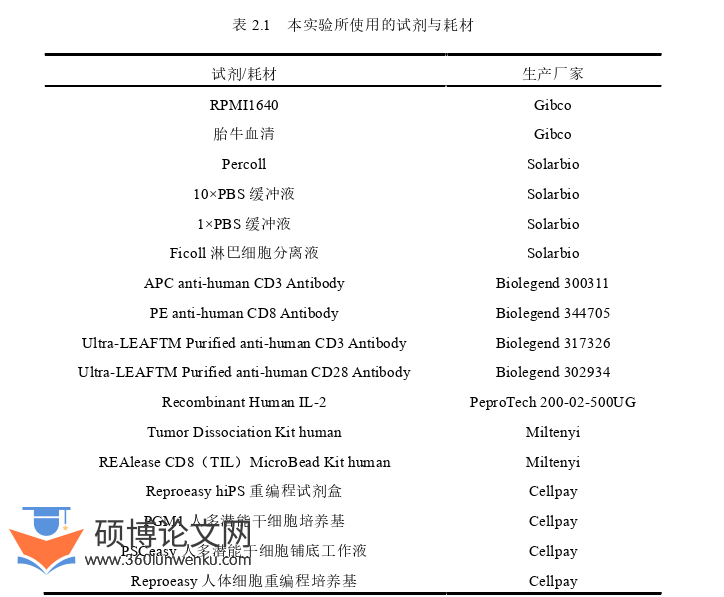
2.2 实验试剂与耗材
临床医学论文怎么写
......................
第三章 实验结果 ............................. 25
3.1 TILS细胞形态 .............................. 25
3.2 TILS细胞数量 .............................. 26
3.3 TILS细胞表型 ....................... 27
第四章 讨论 ................................ 39
4.1 实验结果分析 .......................... 39
4.2 CD8+T细胞耗竭原因分析 ................................. 40
4.3 HCC过继细胞疗法的可行性分析 ........................ 43
第五章 结论 ............................. 47
第四章 讨论
4.1 实验结果分析
实验结果表明,第一,该分离方法可以从每克肿瘤组织中提取出百万数量级别的TILs(106),并且细胞状态良好,生长迅速。第二,从失败的案例中可以找到影响TILs分离的因素。对于原发性肝细胞癌,其肿瘤生长状态直接影响到TILs的生长条件,例如在肿瘤组织脂肪浸润过多或肿瘤内部液化坏死的情况下,无法提取出有用的细胞。当患有HCC与ICC的混合癌时,会导致肿瘤组织十分坚韧,难以解离为单细胞悬液并用密度梯度离心法分离,遇到此类情况选择组织块培养法或许效果更好。第三,通过流式细胞术分析体外分离培养的TILs,结果显示通过该方法提取的TILs中T细胞群中CD8+T细胞比例相比于外周血有具有统计学意义的升高。究其原因可能与肝细胞癌中独特的肿瘤微环境相关,也可能是分离方法导致的差异。前者因TME中细胞间相互作用太过复杂,至今也没有研究清楚,故需要更深入的研究来证实,后者则说明该方法用来研究TILs中的CD8+T细胞亚群有着独特的优势。第四,肝细胞癌发病率男女差异较大,男性往往比女性高3-4倍,实验结果提示男性患者于女性患者肝细胞癌中TILs的CD8+T细胞比例无统计学差异。可能提示患病率的差异并不是由免疫功能差异所导致的。本实验中女性患者来源的肿瘤组织标本仅5例,因样本量过小有可能导致实验结果的偏倚,或许需要更多的女性样本来研究性别之间的TILs的差异。第五,根据流式荧光法检测结果提示,体外培养的T细胞亚群仍有大量分泌TNF-α、IFN-γ等细胞因子的能力,但TILs来源的T细胞分泌IFN-γ的能力相比于外周血来源的T细胞较差。这可能与TILs中T细胞功能受损有关,表现为一种耗竭状态。第六,通过磁珠分选法将体外培养的TILs细胞群中的CD8+细胞筛选出来并单独培养。经过仙台病毒感染后均表现出增殖能力的下降,细胞趋向死亡。重编程均未成功,后来我们尝试改变了细胞数量、病毒感染时离心方式与离心力、更换培养基、共刺激时间延长等多个环节进行了优化,CD8+TILs仍在一周内出现增殖停滞,细胞大部分死亡的情况。除去外部因素影响,这样的结果与重编程试剂盒的选择,HCC来源TILs的特殊性可能是影响重编程的主要因素。
..........................
第五章 结论
(1) 高效HCC-TILs体外分离方法操作便捷、成本低、具有普适性。
(2) 高效HCC-TILs体外分离方法所得TILs数量较多,细胞生长状态更好。与外周血即时分离诱导的T淋巴细胞相比,CD8+T细胞比例较高。
(3) 免疫检查点分子及其配体的表达与HCC息息相关;HCC常用的临床分型标准与免疫检查点的表达水平几乎无关;免疫检查点分子及其配体在TILs中高表达与HCC细胞中低表达与较好的生存率相关。
参考文献(略)
